Un accès équitable aux soins
Les médicaments biosimilaires
Les médicaments biosimilaires : des alternatives biologiques sûres pour un système de santé durable
Un médicament biosimilaire est un médicament biologique dont le brevet du produit de référence (ou « bio-référent ») est arrivé à expiration. Comme tous les médicaments biologiques, il est issu du vivant et se compose de substances complexes comme des protéines, des anticorps, des hormones ou encore des enzymes.
Pour être autorisé en Europe, un biosimilaire doit démontrer qu’il est strictement similaire au médicament de référence sur les plans de la qualité, de la sécurité et de l’efficacité. Cette équivalence est validée à travers une procédure d’autorisation de mise sur le marché (AMM) rigoureuse menée par l’Agence Européenne du Médicament (EMA), puis encadrée par l’ANSM en France. Il est également étroitement surveillé après sa mise sur le marché, garantissant une sécurité d’emploi équivalente à celle du princeps.
Un médicament biologique peut être substitué en pharmacie par n’importe quel biosimilaire listé au sein du groupe des biosimilaires substituables (sauf avis contraire justifié du prescripteur).
« Les médicaments biosimilaires ouvrent de nouvelles perspectives d’accès aux soins et élargissent l’arsenal thérapeutique. Ils sont évalués selon des standards scientifiques les plus exigeants au monde et leur autorisation repose sur une démonstration rigoureuse de similarité avec le médicament de référence. Cette équivalence, validée au niveau européen, est ensuite confirmée par des années d’utilisation en vie réelle. » 1
Une opportunité pour la soutenabilité du système de santé
médicaments biosimilaires
commercialisés en France
d’économies
attendues entre 2026 et 2027
prix moyen
versus 377€ en moyenne en Europe
Un prix bas et un
développement limité
La France se caractérise par un prix moyen du biosimilaire 44% inférieur à celui pratiqué chez nos voisins européens, à savoir l’Allemagne, l’Espagne, l’Italie et le Royaume-Uni. Cette dépréciation de la valeur s’explique par la régulation mise en œuvre chaque année par le Comité économique des produits de santé (CEPS).
PFHT par unité de dispensation des biosimilaires en 2024
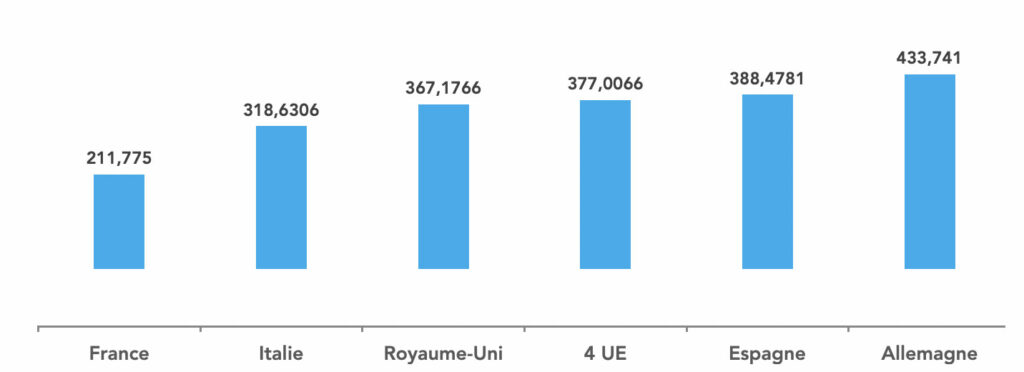
Source ALMA sur la base de données
Part de marché des biosimilaires en 2024
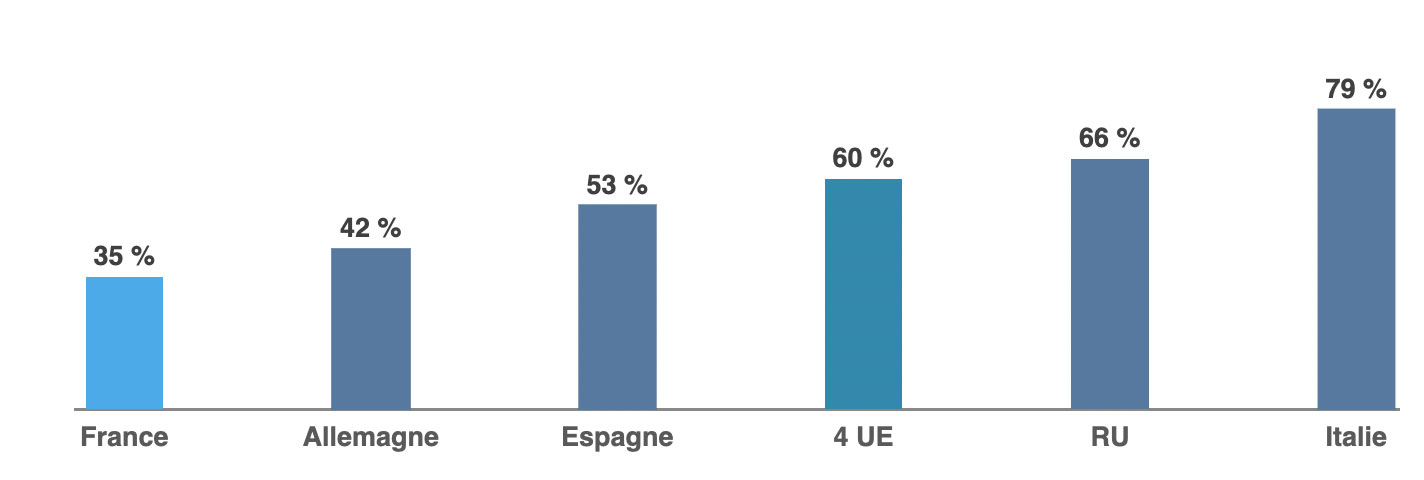
Source ALMA sur la base de données
C’est ainsi que les LFSS successives ont notamment renforcé le recours aux biosimilaires par la substitution officinale : élargissement du périmètre des molécules substituables, réduction du délai d’entrée en vigueur de la substitution, tiers-payant contre biosimilaire, prescription en Dénomination Commune Internationale (DCI)…
1. Grand Angle Santé, « Biosimilaires : la confiance est un enjeu au cœur du parcours de soins » (11 février 2026).
Les médicaments biosimilaires, une adoption à accélerer
Les médicaments biosimilaires sont des traitements à qualité de soin équivalente, sûrs et efficaces. Il est aujourd’hui essentiel de sécuriser et d’accélérer leur adoption pour élargir l’accès aux soins à coût raisonnable au bénéfice des patients, pour maitriser les dépenses de santé et pour réinvestir les économies générées par cette spécialité dans le système de santé.
